
TARİHÇE
Biyoaktif camlar kemiğe tamamen bağlanabilen sentetik biyomalzemelerden biridir. 1960’ların sonlarında Larry L. Hench tarafından geliştirilmiştir. Dr. Hench, Florida Üniversitesi’nde çalışırken, New York Sagamore’da düzenlenen ABD Ordusu Malzeme Araştırma Konferansına katılmak amacıyla çıktığı otobüs yolculuğunda Amerika Birleşik Devletleri’nde görev yapan Albay Klinker’ in ‘‘Yüksek enerjili radyasyona maruz kalmaya dayanacak bir malzeme yapabilirseniz, insan vücuduna maruz kalmaya devam edecek bir malzeme yapabilir misiniz ?’’ sorusu üzerine Hench, vücuttaki dokularla canlı bir bağ oluşturabilecek yeni bir malzemeye ihtiyaç olduğunu fark etmiştir.
Hench konferanstan sonra Florida’ya döndüğünde, ABD Ordusu Tıbbi Araştırma ve Tasarım Komutanlığı’na kemikte bulunan bir hidroksiapatit kaplaması oluşturamadığı sürece metalik veya polimerik malzemeyi reddeden vücut teorisine dayanan bir ürün teklifi sunmuştur. Bunun üzerine 1968’de, ABD Ordusu Tıbbi Araştırma ve Tasarım Komutanlığı’ndan fon aldı ve Kasım 1969’da Hench, 45S5 biyoaktif cam dediği maddenin küçük dikdörtgenlerini sentezlemeye başlamıştır. Ardından ürünü ilk olarak Gainesville’deki VA Hastanesinde sıçan femurlarına implante edilmişitir. Altı hafta sonra hastane yetkilisi Greenlee, Hench’i arayarak, ‘‘Larry, bana verdiğin örnekler neler? Kemikten çıkmayacaklar. Onları çektim, onları ittim, kemiği kırdım ve hala yerinde bağlı.’’ifadesini kullanmıştır. Bu ilk başarılı deney ile biyoaktif cam doğuşu gerçekleşmiş ve ilk kompozisyonlar üzerinde çalışılmıştır.
Hench, konuyla ilgili ilk makalesini 1971’de Journal of Biomedical Materials Research’te yayınlamış ve laboratuvarı, ABD Ordusu’nun sağladığı sürekli fonla önümüzdeki 10 yıl boyunca proje üzerinde çalışmaya devam etmiştir. 2006 yılına kadar, biyoaktif camlar konusunda dünyanın farklı laboratuvarlarından ve kurumlarından 500’ün üzerinde makale yayınlanmıştır.
Biyoaktif cam 45S5’in ilk başarılı cerrahi kullanımı, iletim tipi işitme kaybının tedavisi olarak orta kulaktaki kemikçiklerin yerini almaktı ve materyal günümüzde kemik rekonstrüksiyon uygulamalarında kullanılmaya devam edilmektedir.
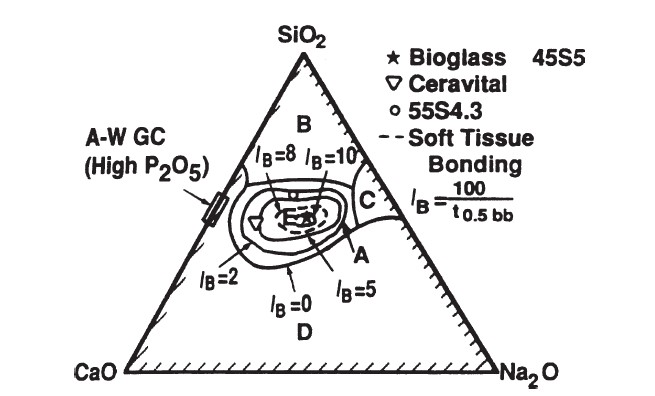
45S5 FAZ DİYAGRAMI
Biyoaktif camlar ve cam seramiklerin kemik bağlanması ve yumuşak doku bağlanmasının bileşimsel bağımlılığı (ağırlıkça % olarak) yukarıdaki faz diyagramında yer almaktadır. A bölgesindeki tüm bileşimler, sabit bir ağırlıkça % 6 P2O5‘e sahiptir. BONE-G ACTIVE®, yukarıda yer alan faz diyagramında ★ ile belirtilen bölgedeki niteliklere sahiptir.
IB, Biyoaktivite indeksi.
★ |
⇒ |
⇒ |
SiO2 : 45 % | |
| BONE-G ACTIVE® | Na2O : 24.5 % | |||
| Bioactive glass 45S5 | CaO : 24.5 % | |||
| P2O5: 6 % |
Kemiğe bağlanabilirliği ile bilinen ilk biyomalzeme grubu olan ve en yaygın haliyle 45S5 olarak bilinen biyoaktif camlar, belirli oranlarda SiO2, Na2O, CaO ve P2O5 bileşimi içerir. 45S5 biyoaktif cam formülasyonu ağırlıkça % 45 SiO2 ve 5: 1 CaO / P2O5 oranını ifade etmektedir.
Biyoaktif camları geleneksel soda-kireç-silika camlardan ayıran üç temel bileşim özelliği vardır. Bunlar, % 60 mol’den az SiO2, yüksek Na2O ve CaO içeriği ve yüksek bir CaO / P2O5 oranı olmasıdır. Bu özellikler sayesinde biyoaktif cam yüzeyi sulu bir ortama maruz kaldığında oldukça reaktif hale gelir. Daha düşük CaO – P2O5 oranlarına sahip camlar kemiğe yapışamazlar. Kemiğe bağlanma işleminde biyoaktif cam yüzeyi, dokularla bağlanma ara yüzü sağlayan biyolojik olarak aktif bir karbonatlanmış HA tabakası (HCA) oluşturur. Bu sayede mekanik kuvvetlere direnen ve dokularla yapışkan bir ara yüz geliştirir.
Kemik ve yumuşak doku bağının Na2O – CaO – P2O5 – SiO2 camlarına bileşimsel bağımlılığı şekildeki faz diyagramında gösterilmektedir. Diyagramdaki tüm camlar, ağırlıkça sabit bir %6 P2O5 oranı içerir. Diyagramda belirtilen A bölgesinde bulunan bileşimler kemik ile kuvvetli bir bağ oluşturabilen seviyede biyoaktivite özelliği sergileyen biyoaktif camlardır. Bu sebeple A bölgesi biyoaktif kemik bağlanma sınırı olarak adlandırılır. B bölgesi kemik ile bağlanma göstermeyen biyoinert camların bölgesi olarak tanımlanmaktadır. Ancak B bölgesi içerisinde bulunan silikat camları eylemsiz malzemeler gibi davranır ve implant-doku ara yüzünde lifli bir kapsül ortaya çıkarır. C bölgesi içindeki camlar ise yeniden emilebilir yapıda olup implantasyondan sonra 10 ila 30 gün içinde kaybolurlar. D bölgesindeki camlar teknik olarak pratik değildir. Bu nedenle implantlar olarak test edilmemiştir. Ayrıca yumuşak dokuların kolajen bileşeni, şekilde gösterilen kesikli çizgi bölgesi içinde yer alan biyoaktif silikat camlara güçlü bir şekilde yapışabilir.
ETKİ MEKANİZMASI
Biyoaktif cam 45S5 implante edildiğinde çevreleyen fizyolojik sıvıyla reaksiyona girerek malzeme yüzeyinde hidroksil karbonatlı apatit (HCA) tabakasının oluşmasına neden olur. HCA tabakası, kemiğin mineral fazı olan hidroksiapatite benzer bir bileşime sahiptir. Kemik ile güçlü etkileşim ve entegrasyona izin veren bir kaliteye sahiptir. Bu reaksiyonun meydana geldiği süreç 12 aşamaya ayrılabilir.
İlk 5 adım, vücut içindeki ortama biyoaktif cam tepkisi ile ilgilidir ve birkaç saat içinde malzeme yüzeyinde hızla gerçekleşir. Reaksiyon adımları 6-10, vücudun biyomateryalin entegrasyonuna verdiği reaksiyonu ve kemikle entegrasyon sürecini detaylandırır. Bu aşamalar, birkaç hafta veya ay boyunca meydana gelir. Adımlar şu şekilde ayrılır:
- Cam yüzeyindeki alkali iyonlar ( Na+ ve Ca2+ ) çevreleyen vücut sıvılarından gelen hidrojen iyonları veya hidronyum ile hızla değiş tokuş edilir. Bu işlem silika gruplarının hidrolizine neden olur, çözeltinin pH’ı artar.
- Yüzeydeki hidroksil (OH-) konsantrasyonundaki artış nedeniyle, Si⎯O⎯Si bağlarının kırılmasıyla görülen silika cam ağında bir çözülme meydana gelir. Çözünür silika Si (OH)4 formuna dönüşür ve malzeme yüzeyinde silanol (Si⎯OH) oluşumu meydana gelir.
- Malzeme yüzeyindeki silanol grupları yoğunlaşır ve biyoaktif cam yüzeyinde bir silika jel tabakası oluşturmak için yeniden polimerize olur.
- Amorf Ca2+ ve PO43− hem çevreleyen vücut sıvısından hem de Bioglass’ın büyük kısmından silika bakımından zengin tabakada toplanır. Bu, silika tabakasının üstünde esas olarak CaO⎯P2O5’ten oluşan bir tabaka oluşur.
- Oluşan CaO⎯P2O5 tabakası, vücut solüsyonundan OH− ve CO32− içerir ve kristalleşmeye neden olur. Bu katmana karışık karbonatlı hidroksil apatit (HCA) denir.
- Hidroksiapatite yapısal ve kimyasal benzerliklerinden dolayı büyüme faktörleri biyoaktif cam yüzeyine adsorbe olur.
- Adsorbe edilen büyüme faktörleri M2 makrofajlarınınaktivasyonuna neden olur . M2 makrofajları, yara iyileşmesini destekleme ve progenitör hücrelerin bir yaralanma bölgesine göçünü başlatma eğilimindedir. Bunun tersine, biyouyumlu olmayan bir materyal implante edildiğinde M1 makrofajları aktive olur ve bir enflamatuar yanıtı tetikler.
- M2 makrofaj aktivasyonu ile tetiklenen mezenkimal kök hücrelerve osteoprogenitör hücreler biyoaktif cam yüzeyine göç eder ve HCA katmanına bağlanır.
- HCA yüzeyindeki kök hücreler ve osteoprogenitör hücreler, tipik olarak kemik dokusunda, özellikle osteoblastlarda bulunan osteojenik hücreler haline gelmek üzere farklılaşır.
- Bağlı ve farklılaşmış osteoblastlar, hücre dışı matris(ECM) bileşenlerini, özellikle kemiğin ana protein bileşeni olan tip I kollajeniüretir ve biriktirir .
- Kolajen ECM ,normal olarak doğal kemikte meydana geldiği gibi mineralizeNano ölçekli hidroksiapatit kristalleri, implant yüzeyinde biriken kolajen ile katmanlı bir yapı oluşturur.
- Bu reaksiyonların ardından, yeni alınan hücreler işlev görmeye ve doku büyümesi ve onarımını kolaylaştırmaya devam ederken kemik büyümesi devam eder. Biyoaktif cam implantı bozulmaya ve yeni ECM materyaline dönüştürülmeye devam eder.
GRAFİKLER VE AÇIKLAMA

Şekil 1 Şekil 2
Doku bağlanma mekanizması, implant-doku arayüzündeki yanıtın tipi ile doğrudan ilişkilidir. Canlı dokuya implante edilen hiçbir materyal inert değildir çünkü tüm materyaller canlı dokulardan bir tepki ortaya çıkarır.
Dört tip doku tepkisi ve iskelet sistemine dört farklı protez takma yolu vardır. Farklı biyoseramik, cam ve cam seramik türlerinin göreceli kimyasal aktivitesinin bir karşılaştırması Şekil 1’ de gösterilmektedir. Şekil1’in A bölgesinde gösterilen kısım göreceli reaktivite kısmına aittir. Göreceli reaktivite, kemik ile seramik, cam veya cam-seramik implantların bir arayüzey bağının oluşum hızı ile yakından ilişkilidir. Bir implantın göreceli reaktivite seviyesi, malzeme ile doku arasındaki ara yüzey bölgesinin veya tabakanın kalınlığını etkiler.
TİP I
Tip I neredeyse inert biyomateryalleri içerir. İnert biyomateryallerin yumuşak ve sert dokularda lifli bir kapsülün hareketi ilerleyen gelişimi vardır. Biyomateryal-doku ara yüzünde hareketin varlığı implantın, arayüzdeki dokunun veya her ikisinin de fonksiyonunda bozulmaya yol açar. Aşınma partikülleri, doku-implant arayüzünün bozulmasını hızlandırabilir. Yapışmayan kapsülün kalınlığı, hem malzemeye hem de bağıl hareketin boyutuna bağlı olarak değişir.
TİP II
Tip II mikro gözenekli inert biyomateryalleri içerir. İnert mikro gözenekli materyallerin kullanımının arkasındaki mekanizma; dokunun, yüzeydeki gözeneklere veya implant boyunca oluşan gözeneklere doğru büyümesidir. İmplant ve dokular arasındaki artan arayüz alanı, cihazın doku içindeki hareketine karşı artan bir dirençle sonuçlanır. Arayüz, gözeneklerdeki canlı doku tarafından oluşturulur. Bu bağlanma yöntemine “biyolojik fiksasyon” adı verilir. “Morfolojik fiksasyonlu” tip 1 implantlardan daha karmaşık stres durumlarına dayanabilir. Tip 2 gözenekli implantlarla ilgili sınırlama, dokunun canlı ve sağlıklı kalması için gözeneklerin 50 ila 150 μm’den büyük olması gerektiğidir. Gözeneklilik için gerekli olan geniş arayüzey alanı, iç içe geçmiş bağ dokusuna bir kan beslemesi sağlama ihtiyacından kaynaklanmaktadır. Ayrıca, gözenekli bir implantın arayüzünde mikro hareket meydana gelirse ve doku hasar görürse kan beslemesi kesilebilir. Bunun sonucunda doku ölümü gerçekleşmiş ve iltihaplanma meydana gelmiş olur. Arayüz stabilitesi yok edilir.
TİPIII
TİP III biyoaktif materyalleri içerir. Biyoaktif materyaller, yeniden emilebilir ve biyoinert materyaller arasında orta düzeydedir. Biyoaktif materyal, materyalin arayüzünde spesifik bir biyolojik tepki ortaya çıkaran, dokular ve materyal arasında bir bağ oluşmasına neden olan materyaldir. Bu malzemelerin tümü, bitişik doku ile bir arayüzey bağ oluşturur. Bununla birlikte, bağlanmanın zamana bağlılığı, bağın gücü, bağlama mekanizması ve bağlama bölgesinin kalınlığı çeşitli malzemeler için farklılık gösterir. Bir biyomateryalin bileşimindeki nispeten küçük değişiklikler, biyoinert, yeniden emilebilir veya biyoaktif olup olmadığını önemli ölçüde etkileyebilir.
TİP IV
TİP IV Emilebilir biyomateryallerdir. Emilebilir biyomateryaller belirli bir süre içinde kademeli olarak bozulabilir ve doğal konak doku ile değiştirilebilir şekilde tasarlanmıştır. Bu olay çok ince veya var olmayan bir arayüz kalınlığına yol açar. Güç ve kısa vadeli performans gereksinimleri karşılanabiliyorsa, optimal biyomateryal çözümdür çünkü doğal dokular yaşam boyunca kendilerini onarabilir ve değiştirebilir. Bu nedenle emilebilir biyomateryaller, biyolojik onarım ilkelerine dayanmaktadır. Büyük miktarlarda malzeme değiştirilebileceğinden, emilebilir bir biyomateryalin yalnızca metabolik olarak kabul edilebilir maddelerden oluşması da önemlidir. Bu kriter, emilebilir biyomalzemelerin bileşimsel tasarımına önemli sınırlamalar getirir.

